1. Sistema Renina-Angiotensina-Aldosterone (SRAA) e ipertensione
Il Sistema Renina-Angiotensina-Aldosterone (SRAA) è un meccanismo ormonale di vitale importanza per la regolazione della pressione sanguigna e l’omeostasi idroelettrolitica. Il sistema viene innescato dalla secrezione dell’enzima renina, prodotto dai reni in risposta a stimoli quali ridotta pressione sanguigna, ipovolemia o scarsità di sodio (1). Al suo rilascio, consegue una reazione a catena che conduce alla produzione di angiotensina II ad opera dell’enzima di conversione dell’angiotensina (ACE), presente nelle cellule endoteliali dei piccoli e grandi vasi. Angiotensina II è un potente vasocostrittore, attiva il sistema simpatico e stimola la secrezione surrenalica di aldosterone con conseguente ritenzione di sodio (1). L’angiotensina II può essere sia circolante che tissutale e si lega a due tipi di recettore definiti recettore dell’angiotensina II di tipo 1 e 2 (AT1 e AT2). Dei due, AT1 – localizzato in tessuti quali muscolatura liscia, cuore, reni, aorta, cervello, adipociti e placenta – è il principale responsabile dell’aumento della pressione sanguigna (3). Al contrario, AT2 controbilancia AT1 favorendo la vasodilatazione, ma la sua espressione sembra essere limitata allo sviluppo fetale o in particolari condizioni di stress, e non è ancora ben chiaro come funzioni l’equilibrio tra l’azione di questi due recettori (4,5). Fondamentale è anche l’azione dell’aldosterone, ormone terminale del SRAA, che regola l’equilibrio dei liquidi corporei e di vari elettroliti, tra cui sodio e potassio (1). Il SRAA regola dunque la pressione sanguigna, mantiene la tonicità vascolare e l’omeostasi idroelettrolitica corporea fondamentale per un corretto funzionamento di cuore e reni, senza rispettivi sovraccarichi (2). Tuttavia, la sua attivazione cronica, in molteplici patologie, comporta svariati effetti negativi, soprattutto a livello cardiovascolare.
L’iperattivazione del SRAA ha un’azione fortemente vasocostrittiva, ipertrofica, pro-fibrotica e pro-infiammatoria, a livello della muscolatura liscia, e conduce all’ipertensione sistemica e al rimodellamento dei tessuti cardiovascolari e renali. Inoltre favorisce l’insorgenza e la progressione del danno cardiovascolare in patologie quali ipertensione, infarto miocardico acuto e insufficienza cardiaca cronica. L’attivazione cronica del SRAA è anche coinvolta nello sviluppo di malattie renali croniche, complicazioni epatiche (alimentate dall’azione pro-infiammatoria), obesità (per l’azione sugli adipociti), diabete e disturbi del sistema nervoso (2). Di fatto, la disregolazione del SRAA alimenta il rischio cardiovascolare e di danno d’organo a cui conseguono eventi clinici anche fatali. Per questa ragione, sono molti i farmaci ideati per agire sull’iperattivazione del SRAA: gli ACE-inibitori impediscono la conversione di angiotensina I in angiotensina II; i sartani bloccano il legame dell’angiotensina II al suo recettore AT1 (per questo noti in inglese come ARBs, Angiotensin II Receptor Blockers); e, infine, gli antagonisti dei recettori dei mineralcorticoidi agiscono a valle, frenando le conseguenze dell’azione dell’aldosterone.
2. Farmaci antipertensivi: antagonisti del recettore dell’angiotensina II o sartani
Il primo antagonista del recettore dell’angiotensina II ad essere approvato è stato Losartan, poi seguito da diversi altri quali Valsartan, Olmesartan, Irbesartan e Candesartan. Come anche gli ACE-inibitori, questi farmaci vengono assunti per via orale ma le differenze nella loro struttura molecolare si traduce in una diversa affinità di legame al recettore e in differenti profili farmacocinetici. I sartani si legano al recettore AT1 impedendo l’interazione con il ligando naturale e riducendo la pressione sanguigna attraverso il rilasciamento della muscolatura liscia dei vasi, l’escrezione di sale e acqua e la riduzione del volume del plasma (6). Nella loro azione antipertensiva, i sartani non alterano gittata e frequenza cardiaca e, nonostante l’abbassamento della pressione, non sembrano indurre ipotensione posturale (3). La dissociazione dal recettore è molto lenta, fattore da tenere in considerazione nella farmacocinetica del principio attivo (7). La maggior parte dei sartani commercialmente disponibili controlla la pressione sanguigna sulle 24 ore anche con una singola somministrazione giornaliera, senza alterare il ritmo circadiano, e la loro efficacia persiste nei trattamenti a lungo termine, senza evidenze di tachifilassi (6). I sartani apportano svariati benefici cardiovascolari tra cui: 1) riduzione dell’ipertrofia ventricolare sinistra, 2) miglioramento della funzione diastolica, 3) riduzione della dispersione anomala del QT nell’elettrocardiogramma, 4) miglioramento della disfunzione endoteliale e 5) miglioramento della capacitanza delle grandi arterie (6). I sartani sono infatti raccomandati nei pazienti con scompenso cardiaco e frazione di eiezione ridotta intolleranti agli ACE-inibitori. Lo studio Val-HeFT ha mostrato come l’aggiunta di Valsartan alla terapia standard riducesse le ospedalizzazioni per scompenso e, nello studio CHARM-Alternative, Candesartan ha ridotto sia le ospedalizzazioni per scompenso che la mortalità cardiovascolare. L’unico dei sartani ad essere impiegato nella gestione dei pazienti che hanno subito un recente infarto del miocardio è Valsartan, che nello studio VALIANT ha dimostrato un’efficacia sovrapponibile a quella di un ACE-inibitore.
I sartani sono stati sviluppati per superare alcuni limiti del meccanismo d’azione degli ACE-inibitori, che infatti modulano la produzione di angiotensina II, impedendo la conversione da angiotensina I, ma falliscono nel sopprimerne la produzione da parte di vie enzimatiche alternative (3). Inoltre, gli ACE-inibitori sono causa di un aumento della concentrazione plasmatica di bradichinina, fattore correlato ad alcuni degli effetti collaterali tipici quali tosse secca e rischio di angioedema. Quest’ultima è una reazione rara, ma comunque pericolosa, che può manifestarsi nelle prime settimane di terapia. Rispetto agli ACE-inibitori, i sartani agiscono più a valle e sono associati ad un minor rischio – ma non nullo – di tosse secca e angioedema (7). L’efficacia dei sartani è pari a quella degli ACE-inibitori nel trattamento contro l’ipertensione, sia moderata che severa, e cresce all’aumentare della dose. A inizio terapia, i sartani possono apparire meno efficaci degli ACE-inibitori, in cui però il rischio di ipotensione iniziale è maggiore (7).
Gli antagonisti del recettore dell’angiotensina II sono generalmente farmaci ben tollerati: non compromettono la regolazione del flusso ematico cerebrale, il metabolismo del glucosio o dei lipidi, non provocano alterazioni clinicamente significative delle misure di laboratorio di chimica del siero, ematologia e analisi delle urine (6). Il trattamento con sartani prevede l’impiego di una dose iniziale che va poi titolata a raggiungimento della dose target o del massimo dosaggio tollerato. Il loro utilizzo richiede cautela nei pazienti affetti da malattia renale cronica e insufficienza cardiaca, o diabete, e che ricevono diuretici risparmiatori di potassio o integratori di potassio, poiché possono causare iperkaliemia (7). Nei pazienti trattati con sartani da lungo tempo, è importante considerare che l’interruzione brusca della terapia può causare un improvviso aumento della pressione. Alcuni effetti collaterali comuni sono mal di testa, vertigine, astenia e infiammazione delle vie respiratorie superiori (5). I sartani sono infine sconsigliati in gravidanza a causa della loro tossicità fetale.
3. Losartan
3.1. Indicazioni e posologia
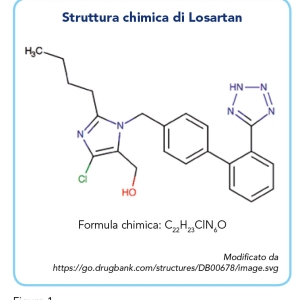
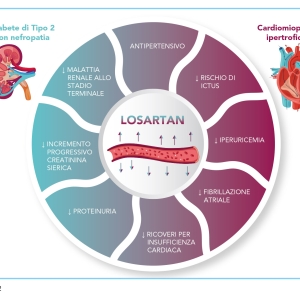
Losartan è stato il primo farmaco bloccante del recettore AT1 ad essere sintetizzato, alla fine degli anni ‘90, a partire da un gruppo di molecole con debole attività antagonista nei confronti di questo recettore (Figura 1) (3,8). Il suo utilizzo è indicato per il trattamento dell’ipertensione essenziale in adulti, anziani, bambini e adolescenti (6-18 anni). Nel contesto della terapia antipertensiva, Losartan è adoperato per la protezione renale in pazienti con diabete di tipo 2 con proteinuria ≥ 0,5 g/die e la riduzione del rischio di ictus nei pazienti con ipertrofia ventricolare sinistra. Questo farmaco è inoltre adeguato al trattamento dell’insufficienza cardiaca cronica nei pazienti adulti non eleggibili al trattamento con ACE-inibitori, purché questi non siano stati precedentemente stabilizzati con un ACE-inibitore, abbiano una frazione d’eiezione sinistra ≤ 40% e siano clinicamente stabili. Infine, Losartan è in grado di ridurre i livelli sierici dell’acido urico – un importante fattore di rischio per le malattie cardiovascolari e renali – attraverso la sua azione sul trasporto dell’urato nel tubulo renale che avviene indipendentemente dal blocco di AT1 (9–11).
Come si evince dal riassunto delle caratteristiche del farmaco fornite da AIFA (Agenzia Italiana del Farmaco), Losartan viene abitualmente somministrato con una monodose giornaliera ed è efficace nell’arco delle 24 ore. Nei pazienti ipertesi, il trattamento iniziale è di 50 mg e raggiunge la massima efficacia dopo 3-6 settimane. Alcuni pazienti possono trarre ulteriore beneficio con un aumento della dose a 100 mg (assunzione mattutina). Losartan può essere somministrato parallelamente ad altri agenti ipertensivi (calcio-antagonisti, alfa o beta bloccanti, farmaci a meccanismo d’azione centrale) e, in particolare, diuretici (e.g. idroclorotiazide) per ottenere un effetto sinergico sull’ipertensione. Questo stesso protocollo di trattamento può essere applicato per la riduzione del rischio di complicazioni nei pazienti ipertesi con accertata ipertrofia ventricolare sinistra o con diabete di tipo 2 e proteinuria ≥ 0,5 g/die. Nel caso di pazienti diabetici, non vi è controindicazione nell’utilizzo di Losartan parallelamente a insulina e farmaci ipoglicemizzanti (sulfaniluree, glitazoni e inibitori della glicosidasi), si consiglia però di attendere un mese dall’inizio del trattamento per aumentare la dose a 100 mg. Nel trattamento dell’insufficienza cardiaca, Losartan viene abitualmente fornito in una monodose iniziale di 12,5 mg/giorno. Il dosaggio va poi titolato ad intervalli settimanali fino ad un massimo di 150 mg, in base alla tollerabilità del paziente.
Sono presenti tre categorie speciali che richiedono attenzione particolare nell’utilizzo di questo sartano: 1) i pazienti con deplezione di volume intravascolare, in cui si consiglia una dose iniziale di 25 mg; 2) i pazienti con compromissione renale e in emodialisi, in cui non è necessario alcun aggiustamento iniziale ma è raccomandato uno stretto monitoraggio della funzionalità dei reni; e 3) i pazienti con problematiche epatiche, in cui il farmaco è controindicato se il danno presente è grave, o se ne consiglia un abbassamento della dose se il paziente ha storia di compromissione epatica. Nei casi di cirrosi epatica, c’è rischio di un aumento della concentrazione plasmatica di Losartan, si consiglia dunque di considerare un dosaggio inferiore.
Nei pazienti pediatrici dai 6 ai 18 anni si può somministrare Losartan in dosi proporzionate al peso: 25 mg tra i 20 e i 50 kg e 50 mg oltre i 50 kg (in casi eccezionali la dose può essere raddoppiata per entrambe le categorie). Dosaggi superiori a 1,4 mg/kg o superiori a 100 mg non sono stati studiati nei pazienti pediatrici e non è stata stabilita la sicurezza del farmaco per bambini tra i 6 mesi e i 6 anni. Losartan non è raccomandato nei pazienti pediatrici con compromissione epatica o con tasso di filtrazione glomerulare < 30 mL/min/1,73 m2. Nei pazienti anziani non è generalmente necessario un aggiustamento del dosaggio, ma si può valutare di ridurre la terapia iniziale a 25 mg se di età superiore ai 75 anni.
3.2. Meccanismo d’azione
Losartan è un antagonista competitivo, reversibile e selettivo del recettore AT1 che coopera con il suo metabolita attivo E-3174 per indurre un potente effetto antipertensivo. Si tratta di una molecola non peptidica con una struttura tetrazolo-bifenilica (Figura 1), simile a Valsartan (6). La concentrazione di Losartan necessaria a inibire il 50% del bersaglio (IC50) corrisponde a 20 nmol/L (8). Dopo 24 ore dalla somministrazione, la sua efficacia antipertensiva è pari al 70-80% dell’effetto osservato a 5–6 ore, viene perciò assunto in monodose giornaliera. L’abbassamento della pressione avviene in misura simile a farmaci quali enalapril, atenololo e felodipina a rilascio prolungato (12). Il metabolita attivo è un acido carbossilico che agisce come antagonista reversibile non competitivo del recettore AT1 e la cui attività, a parità di peso, è dalle 10 alle 40 volte maggiore a quella di Losartan (13). Entrambi mostrano un’elevata affinità per il recettore AT1, di molto maggiore a quella per AT2, impedendo l’interazione con l’angiotensina II e la conseguente vasocostrizione, il rilascio di aldosterone e la proliferazione delle cellule muscolari lisce. Losartan è in grado di mantenere un blocco efficace del recettore AT1 nonostante l’incremento plasmatico dell’angiotensina II dovuto al mancato feedback negativo sull’attività della renina, enzima a monte della cascata di reazioni del SRAA. A seguito dell’interruzione di una terapia con Losartan, i valori di renina e angiotensina II tornano normali entro 3 giorni. Losartan non agisce su ACE, eludendo gli effetti collaterali mediati dall’aumento di bradichina tipici degli ACE-inibitori, e non ha effetto agonista su recettori ormonali o canali ionici implicati nella regolazione cardiovascolare. Alcuni studi hanno invece riportato un effetto inibitorio di Losartan sull’attivazione e sull’aggregazione piastrinica attraverso l’antagonismo dei recettori del trombossano A2 (13).
3.3. Farmacocinetica
Losartan è un farmaco a somministrazione orale che può essere assunto indipendentemente dai pasti e rapidamente assorbito a livello gastrointestinale. Losartan subisce un metabolismo di primo passaggio e il 14% della dose viene trasformata nel metabolita farmacologicamente attivo E-3174; questa conversione è assente solo nell’1% degli individui (6). La farmacocinetica dei due principi farmacologicamente attivi è lineare, proporzionale alla dose e non cambia sostanzialmente con la somministrazione ripetuta (12). La biodisponibilità sistemica di Losartan in compresse è di ~33% (intervallo 29-43%) con picchi medi di concentrazione di 1 ora per Losartan e 3–4 ore per il suo metabolita attivo (6). Il volume di distribuzione di Losartan è di 34 L e si lega abbondantemente alle proteine plasmatiche (≥ 99%), in particolare all’albumina. Il metabolismo di Losartan passa attraverso gli isoenzimi del citocromo P450 (CYP) 3A4, 2C9 e 2C10 (12). L’inibizione dell’isoforma CYP2C9 con fluconazolo diminuisce del 50% l’esposizione al metabolita attivo, mentre il trattamento con rifampicina (induttore degli enzimi metabolici) riduce del 40% la concentrazione plasmatica del metabolita attivo, senza rilevanze cliniche conosciute. Oltre al metabolita attivo, Losartan viene biotrasformato in altri metaboliti però inattivi. L’eliminazione di Losartan e i suoi metaboliti avviene per via biliare e urinaria; nello specifico, il 4-5% di Losartan viene escreto in forma invariata tramite le urine, mentre il suo metabolita attivo mostra il 6-8% di eliminazione per questa via (6). Tra il 50 e il 58% del farmaco, in tutti i suoi sottoprodotti, fuoriesce per via fecale quando somministrato per via intravenosa; questa percentuale sale al 65% se assunto oralmente (6). La clearance di Losartan e del suo metabolita attivo sono rispettivamente 610 mL/min e 50 mL/min per quella plasmatica, e 72 mL/min e 25,9 mL/min per quella renale (13). Nei pazienti con clearance di creatinina > 10 mL/min le concentrazioni plasmatiche di Losartan rimangono invariate mentre, se i pazienti sono in emodialisi, l’AUC del farmaco è due volte maggiore (senza variazioni per il metabolita attivo). Nei pazienti con cirrosi alcolica, la biodisponibilità di Losartan aumenta inducendo un incremento dalle 4 alle 5 volte della concentrazione plasmatica (13). L’emivita di Losartan e del suo metabolita attivo corrispondono a 2 e 6–9 ore rispettivamente, con una riduzione poliesponenziale della loro concentrazione plasmatica dal momento dell’assunzione orale. Losartan non presenta interazioni farmacocinetiche con l’idroclorotiazide, la digossina o la warfarina (13).
3.4. Sicurezza e tollerabilità
Losartan è un farmaco molto ben tollerato nei pazienti ipertesi e, stando al riassunto delle caratteristiche di questo farmaco fornite da AIFA, gli effetti avversi più frequentemente riportati (≥ 1%) sono solo capogiri e vertigini; è inoltre raro osservare ipotensione da prima dose. È stata segnalata una riduzione di emoglobina ed ematocrito nella terapia con Losartan, senza comportare particolari effetti clinici (9). Altri effetti secondari – come anemia, astenia, affaticamento e compromissione renale – possono emergere con più frequenza in popolazioni con problematiche cardiovascolari o metaboliche. Sono anche stati segnalati alcuni casi di angioedema coincidenti all’utilizzo di Losartan.
Losartan è controindicato 1) in casi di ipersensibilità al principio attivo o ad uno dei suoi eccipienti, 2) nel secondo e terzo trimestre di gravidanza a causa della sua tossicità fetale e neonatale, 3) nei casi di grave compromissione epatica e 4) nei pazienti con diabete mellito o compromissione renale che ricevono medicinali contenenti aliskiren a causa dell’aumento degli effetti avversi osservati in occasione dello studio ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) (14).
A causa dell’azione di Losartan sul SRAA, si consiglia di prestare attenzione a tutte quelle condizioni che comportano uno squilibrio elettrolitico, in particolar modo in presenza di compromissione renale, con o senza diabete. Poiché c’è rischio si verifichi ipotensione sintomatica in pazienti volume- e/o sodio-depleti, si raccomanda di correggere questa condizione prima di somministrare Losartan oppure di introdurlo ad un dosaggio più basso. La concentrazione plasmatica di potassio va tenuta monitorata, come anche i livelli di clearance della creatinina, in particolare nei pazienti con scompenso cardiaco. Come per altri sartani, l’uso concomitante con sostanze che favoriscono la ritenzione del potassio o ne aumentano i livelli sierici (e.g. diuretici risparmiatori di potassio, integratori di potassio, sostituti dei sale contenenti potassio ma anche eparina) non è raccomandato. Sono inoltre stati riportati aumenti sierici reversibili della concentrazione e tossicità del litio in utilizzo concomitante di Losartan e ACE-inibitori.
L’azione sul SRAA attuata da Losartan può inoltre riverberare sulla funzionalità renale fino a causare – nei casi più gravi – insufficienza renale anche acuta, in particolar modo nei pazienti con scompenso cardiaco o disfunzione renale pregressa. Per questa ragione, si consiglia prudenza in questi casi oltre che in presenza di febbre e disidratazione. Sono stati riportati aumenti dell’urea ematica e della creatinina sierica nei pazienti con stenosi bilaterale dell’arteria renale o dell’arteria tributaria di un rene unico, Losartan va dunque utilizzato con cautela in tali pazienti.
Losartan, come anche altri medicinali che agiscono sul SRAA, può causare ipotensione grave nei pazienti con ischemia cardiovascolare, malattia cerebrovascolare e scompenso cardiaco – specie se concomitanti a condizioni di compromissione renale grave o aritmie cardiache sintomatiche. L’azione simultanea di Losartan e antidepressivi triciclici, antipsicotici, baclofene e amifostina può anch’essa causare ipotensione sintomatica. Contrariamente, l’utilizzo concomitante di FANS (farmaci antinfiammatori non steroidei) può attenuare l’effetto antipertensivo, oltre che aumentare il rischio di problematiche renali ed elettrolitiche. Nei pazienti di etnia africana è stata riportata un’inferiore efficacia antipertensiva dei sartani probabilmente dovuta a una ridotta espressione della renina. Infine, l’interruzione di Losartan può portare a una brusca ipertensione da rebound con pericolose conseguenze cardiovascolari.
Studi più rilevanti:
• Losartan riduce il rischio di eventi cardiovascolari nei pazienti con ipertrofia ventricolare sinistra
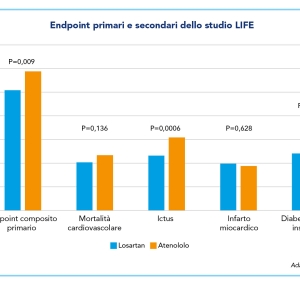
Lo studio LIFE (Losartan Hypertension Survival Study) è stato uno degli studi portanti della terapia con Losartan. Iniziato negli anni ’90, ha coinvolto 9.193 partecipanti di età compresa tra i 55 e gli 88 anni e con ipertensione essenziale e segni d’ipertrofia ventricolare sinistra. Lo scopo dello studio era quello di determinare se il blocco del recettore AT1, attuato da Losartan, riducesse il rischio di morbilità e mortalità cardiovascolare in questi pazienti (15). Il farmaco comparativo utilizzato in questo studio è l’atenololo, un beta-bloccante in prima linea nel trattamento dell’ipertensione. La terapia antipertensiva, randomizzata con Losartan o atenololo, poteva ricevere un’aggiunta di idroclorotiazide o un raddoppiamento della dose al fine di raggiungere valori pressori target < 140/90 mmHg (sistolica/diastolica). Il follow-up medio dei pazienti è stato di 4,8 anni e sono stati confrontati il numero di eventi cardiovascolari primari (morte, infarto o ictus) nei due gruppi. Si è innanzitutto osservato un abbassamento della pressione sistolica/diastolica simile tra Losartan e atenololo (-30,2/-16,6 mmHg vs -29,1/-16,8 mmHg che ha portato ad una media finale di 144,1/81,3 mmHg e 145,4/80,9 mmHg, rispettivamente). I valori pressori target sono stati raggiunti dal 48% dei pazienti nel caso di Losartan, e dal 45% nel caso di atenololo. Losartan ha mostrato il 13% di riduzione del rischio di eventi cardiovascolari primari rispetto a atenololo, di cui il più evidente risulta essere il rischio di ictus, ridotto del 24,9% (P<0,001), mentre la mortalità per altre cause cardiovascolari e il rischio di infarto miocardico fatale e non fatale erano simili nei due gruppi (Figura 3) (15). L’utilizzo di Losartan si è rivelato estremamente utile per ridurre i livelli sierici di acido urico (P=0,004), risultati del 29% inferiori rispetto al gruppo con atenololo. I pazienti con ipertensione e iperuricemia hanno un rischio da 3 a 5 volte maggiore di andare incontro a malattia coronarica o cerebrovascolare rispetto ai pazienti con livelli normali di acido urico (4). È stata, infine, osservata una riduzione d’insorgenza di diabete del 25% e di fibrillazione atriale del 21% nel gruppo trattato con Losartan (15,16). Si è perciò dedotto che Losartan, a parità di efficacia antipertensiva, è più efficace del beta-bloccante di confronto nel ridurre morbilità e mortalità cardiovascolare in questa popolazione. È inoltre rilevante menzionare che Losartan ha mostrato un miglior profilo di tollerabilità rispetto a atenololo, con un’inferiore incidenza di effetti avversi.
Poiché la scelta del farmaco ipertensivo dipende anche dall’età del paziente, si è approfondita l’efficacia del trattamento confrontando gli esiti di pazienti di età inferiore/superiore a 67 anni (17). Losartan ha mostrato un maggiore effetto antipertensivo nel gruppo di pazienti più anziani indipendentemente dai fattori di rischio cardiovascolari. Un’approfondita analisi dello studio LIFE e di altre pubblicazioni successive afferma che Losartan attenua il rischio tromboembolico agendo su una pluralità di meccanismi quali il rimodellamento/ingrandimento cardiaco e vascolare, la disfunzione endoteliale, la fibrillazione atriale e la formazione di trombi (18). Proiettando gli esiti di Losartan sulla popolazione europea stimata di pazienti con ipertensione e ipertrofia ventricolare sinistra, si è riscontrato che Losartan fosse potenzialmente in grado di prevenire quasi 125.000 primi ictus entro 5,5 anni (19).
• Studio RENAAL: la protezione dal danno renale di Losartan nei pazienti diabetici con nefropatia
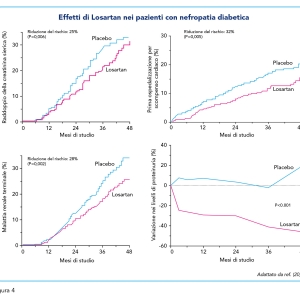
Lo studio RENAAL (Reduction of Endpoints in NIDDM – Non Insuline Dependent Diabetes Mellitus – with the Angiotensin II Antagonist Losartan) è stato ideato per valutare l’efficacia di Losartan nei pazienti affetti da diabete di tipo 2 e conseguente nefropatia diabetica (20). Sono stati coinvolti 1.513 pazienti, randomizzati in una terapia con Losartan o placebo (da 50 a 100 mg una volta al giorno), in aggiunta al trattamento antipertensivo convenzionale (calcio antagonisti, diuretici, alfa e beta-bloccanti e altri agenti ad azione centrale), e seguiti per una media di 3,4 anni. Sebbene a fine studio i tassi di mortalità non differissero tra i due gruppi, Losartan si è dimostrato in grado di ridurre del 25% l’incidenza del raddoppio della creatinina sierica (P=0,006), del 35% il livello di proteinuria (P<0,001) e del 28% il rischio di malattia renale allo stadio terminale (P=0,002) (Figura 4). Gli autori hanno poi stimato che una tale riduzione del rischio renale comportasse un ritardo medio di due anni nella necessità di dialisi o trapianto (20). È stata inoltre riscontrata una piccola differenza negli esiti di pressione arteriosa tra Losartan e placebo (140/74 mmHg vs 142/74 mmHg a fine studio), ma la correzione statistica ha confermato che la protezione renale osservata non fosse attribuibile a tale differenza. La morbilità e la mortalità per cause cardiovascolari sono risultate simili nei due gruppi, anche se il tasso di prima ospedalizzazione per insufficienza cardiaca è risultato inferiore del 32% nel gruppo trattato con Losartan (P=0,005) (Figura 4). Questo dato è stato poi riconfermato anche da una successiva meta-analisi che integra allo studio RENAAL i dati di pazienti diabetici dello studio LIFE (21). Per quanto riguarda la tollerabilità del farmaco, Losartan e placebo, entrambi sommati alla terapia antipertensiva convenzionale, hanno mostrato simile frequenza d’interruzione del trattamento a causa di effetti avversi (7,5% vs 7,8%). L’aggiunta di Losartan al regime di trattamento antipertensivo convenzionale non ha aumentato l’incidenza di eventi avversi. In sintesi, nei pazienti con diabete di tipo 2 e nefropatia, Losartan ha portato a un significativo miglioramento e protezione renale che va oltre quello attribuibile al controllo della pressione arteriosa e con un eccellente profilo di tollerabilità.
• Losartan nel trattamento dello scompenso cardiaco: esiti di tre studi
L’utilizzo terapeutico di Losartan nel trattamento allo scompenso cardiaco, in particolare nei pazienti con frazione di eiezione ≤ 40%, è stato approfondito tramite vari studi. Il primo di questi è lo studio ELITE (Evalution of Losartan in the Elderly), attuato in una coorte di 722 pazienti anziani con insufficienza cardiaca sintomatica (22). Lo scopo era quello di comparare gli esiti di un farmaco ACE-inibitore, captopril, a Losartan in pazienti che non avevano mai assunto alcuno dei due farmaci. Lo studio, della durata di 48 settimane, ha mostrato una significativa riduzione della mortalità e delle ospedalizzazioni con l’utilizzo dell’antagonista del recettore AT1 rispetto a captopril, esito che ha motivato gli autori ad ampliare lo studio in quello che è stato poi definito lo studio ELITE II. ELITE II ha arruolato 3.152 pazienti (> 60 anni) con insufficienza cardiaca di classe II-IV e frazione d’eiezione ≤ 40% (23). I pazienti sono stati randomizzati a Losartan 50 mg/giorno (n=1.578) o captopril 50 mg tre volte al giorno (n=1.574). Il tempo mediano di follow-up è stato di 1,5 anni per ciascun gruppo. Nonostante gli esiti dello studio pilota, ELITE II non ha mostrato significative differenze nel tasso di mortalità media annuale per tutte le cause tra i due gruppi (11,7% vs 10,4%) o nell’insieme di morte improvvisa e arresti per rianimazione (9,0% vs 7,3%). È possibile che questa differenza tra ELITE e ELITE II derivasse dal ristretto numero di morti osservate nel primo studio; lo studio ELITE II ha valutato 4 volte più pazienti e 10 volte il numero di eventi (23). Un risultato importante di questo studio è stato quello di valutare i benefici della terapia con Losartan a livello di effetti collaterali. Infatti, il tasso di abbandono dello studio per effetti avversi è risultato significativamente inferiore nel gruppo Losartan (9,7% vs 14,7; P<0,001), questo includeva anche la tosse, conseguenza tipica del trattamento con ACE-inibitori (Figura 5). In luce a questi risultati, si è concluso che Losartan sia consigliato nei pazienti con scompenso cardiaco nei casi di incompatibilità d’utilizzo degli ACE-inibitori.
Un altro studio successivo, chiamato HEAAL (Heart failure Endpoint evaluation of Angiotensin II Antagonist Losartan), ha valutato gli effetti di Losartan a varie dosi nei pazienti con scompenso cardiaco, frazione d’eiezione ridotta e intolleranza agli ACE-inibitori (24). 1.927 pazienti sono stati randomizzati alla dose di 150 mg e 1.919 alla dose di 50 mg; la mediana di follow-up è stata di 4,7 anni in ciascun gruppo. I pazienti deceduti sono stati 635 durante il trattamento con la dose a 150 mg e 665 per la dose a 50 mg (HR: 0,94; 95% CI: 0,84–1,04; p=0,24). I pazienti ricoverati per insufficienza cardiaca sono risultati essere il 13% meno nella terapia con 150 mg (450 vs 503; HR: 0,87; 95% CI: 0,76–0,98; P=0,025), questa percentuale aumentava al 72% nei pazienti trattati parallelamente con beta-bloccanti (24). È fondamentale sottolineare che l’incidenza di ipotensione, iperkaliemia e insufficienza renale siano anch’essi risultati maggiori nella terapia con Losartan a 150 mg, sebbene questo non abbia causato un aumento significativo dell’abbandono della terapia. Questo studio evidenzia come l’aumento della dose di Losartan migliori gli esiti clinici dei pazienti con scompenso cardiaco intolleranti agli ACE-inibitori ma sia necessario monitorare con attenzione i livelli di pressione sanguigna, gli elettroliti nel siero e la funzionalità renale.
Conclusioni
Losartan è un efficace farmaco antipertensivo che ha fatto da apripista nella terapia con antagonisti del recettore AT1. Grazie alla sua azione a lunga durata, può essere somministrato in monosomministrazione giornaliera sia ad adulti che giovani (da 6 anni) e anziani. Ha un’eccellente profilo di tollerabilità e può essere usato nei pazienti che soffrono d’intolleranza verso gli ACE-inibitori, mentre si consiglia cautela nei pazienti con problematiche renali e epatiche. Losartan è controindicato nel secondo e terzo trimestre di gravidanza per possibile tossicità fetale. Losartan ha mostrato notevoli capacità cardio e nefroprotettive in varie popolazioni. Ad esempio, a parità di azione antipertensiva, lo studio LIFE ha mostrato che Losartan riduce del 25% il rischio di ictus nei pazienti con ipertrofia ventricolare sinistra rispetto al trattamento con un beta-bloccante, riduce inoltre l’incidenza di fibrillazione atriale del 21% e l’insorgenza di diabete del 25% (15-16). Questo studio ha anche mostrato una riduzione del 29% per livelli sierici di acido urico, un importante fattore di rischio cardiovascolare. Nei pazienti con diabete di tipo 2, Losartan protegge la funzionalità renale contrastando l’aumento della creatinina sierica e la proteinuria; il rischio di malattia renale terminale in tali pazienti risulta ridotta del 28% e la probabilità di prima ospedalizzazione per scompenso cardiaco scende del 32% (20). Losartan può essere infine utilizzato nel trattamento dei pazienti con insufficienza cardiaca e frazione di eiezione ridotta, quando intolleranti agli ACE-inibitori, con esiti simili a livello di prevenzione della mortalità cardiaca (23). In tali pazienti un aumento della dose da 50 a 150 mg può apportare benefici cardiovascolari prestando attenzione ai parametri degli elettroliti sierici e di funzionalità renale (24).
Bibliografia
- Ames MK, Atkins CE, Pitt B. The renin-angiotensin-aldosterone system and its suppression. J Vet Intern Med. 2019 Mar;33(2):363–82.
- Patel S, Rauf A, Khan H, Abu-Izneid T. Renin-angiotensin-aldosterone (RAAS): The ubiquitous system for homeostasis and pathologies. Biomed Pharmacother. 2017 Oct;94:317–25.
- Laurent S. Antihypertensive drugs. Pharmacol Res. 2017 Oct;124:116–25.
- Ram CVS. Angiotensin receptor blockers: current status and future prospects. Am J Med. 2008 Aug;121(8):656–63.
- Hernández-Hernández R, Sosa-Canache B, Velasco M, Armas-Hernández MJ, Armas-Padilla MC, Cammarata R. Angiotensin II receptor antagonists role in arterial hypertension. J Hum Hypertens. 2002 Mar;16 Suppl 1:S93-99.
- Israili ZH. Clinical pharmacokinetics of angiotensin II (AT1) receptor blockers in hypertension. J Hum Hypertens. 2000 Apr;14 Suppl 1:S73-86.
- Dina R, Jafari M. Angiotensin II-receptor antagonists: an overview. Am J Health Syst Pharm. 2000 Jul 1;57(13):1231–41.
- Burnier M, Brunner HR. Angiotensin II receptor antagonists. Lancet. 2000 Feb 19;355(9204):637–45.
- Sica DA, Gehr TWB, Ghosh S. Clinical pharmacokinetics of losartan. Clin Pharmacokinet. 2005;44(8):797–814.
- Alderman M, Aiyer KJV. Uric acid: role in cardiovascular disease and effects of losartan. Curr Med Res Opin. 2004 Mar;20(3):369–79.
- Burnier M. Angiotensin II type 1 receptor blockers. Circulation. 2001 Feb 13;103(6):904–12.
- Al-Majed ARA, Assiri E, Khalil NY, Abdel-Aziz HA. Losartan: Comprehensive Profile. Profiles Drug Subst Excip Relat Methodol. 2015;40:159–94.
- Moen MD, Wagstaff AJ. Losartan: a review of its use in stroke risk reduction in patients with hypertension and left ventricular hypertrophy. Drugs. 2005;65(18):2657–74.
- Parving HH, Brenner BM, McMurray JJV, de Zeeuw D, Haffner SM, Solomon SD, et al. Cardiorenal End Points in a Trial of Aliskiren for Type 2 Diabetes. New England Journal of Medicine. 2012 Dec 6;367(23):2204–13.
- Dahlöf B, Devereux RB, Kjeldsen SE, Julius S, Beevers G, de Faire U, et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet. 2002 Mar 23;359(9311):995–1003.
- Wachtell K, Lehto M, Gerdts E, Olsen MH, Hornestam B, Dahlöf B, et al. Angiotensin II receptor blockade reduces new-onset atrial fibrillation and subsequent stroke compared to atenolol: the Losartan Intervention For End Point Reduction in Hypertension (LIFE) study. J Am Coll Cardiol. 2005 Mar 1;45(5):712–9.
- Ruwald ACH, Westergaard B, Sehestedt T, Kjeldsen SE, Lindholm LH, Wachtell K, et al. Losartan versus atenolol-based antihypertensive treatment reduces cardiovascular events especially well in elderly patients: the Losartan Intervention For Endpoint reduction in hypertension (LIFE) study. J Hypertens. 2012 Jun;30(6):1252–9.
- Devereux RB, Dahlöf B. Potential mechanisms of stroke benefit favoring losartan in the Losartan Intervention For Endpoint reduction in hypertension (LIFE) study. Curr Med Res Opin. 2007 Feb;23(2):443–57.
- Katsiki N, Tsioufis K, Ural D, Volpe M. Fifteen years of LIFE (Losartan Intervention for Endpoint Reduction in Hypertension)—Lessons learned for losartan: An “old dog playing good tricks.” The Journal of Clinical Hypertension. 2018;20(8):1153–9.
- Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH, et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med. 2001 Sep 20;345(12):861–9.
- Carr AA, Kowey PR, Devereux RB, Brenner BM, Dahlöf B, Ibsen H, et al. Hospitalizations for new heart failure among subjects with diabetes mellitus in the RENAAL and LIFE studies. Am J Cardiol. 2005 Dec 1;96(11):1530–6.
- Pitt B, Segal R, Martinez FA, Meurers G, Cowley AJ, Thomas I, et al. Randomised trial of losartan versus captopril in patients over 65 with heart failure (Evaluation of Losartan in the Elderly Study, ELITE). Lancet. 1997 Mar 15;349(9054):747–52.
- Pitt B, Poole-Wilson PA, Segal R, Martinez FA, Dickstein K, Camm AJ, et al. Effect of losartan compared with captopril on mortality in patients with symptomatic heart failure: randomised trial–the Losartan Heart Failure Survival Study ELITE II. Lancet. 2000 May 6;355(9215):1582–7.
- Konstam MA, Neaton JD, Dickstein K, Drexler H, Komajda M, Martinez FA, et al. Effects of high-dose versus low-dose losartan on clinical outcomes in patients with heart failure (HEAAL study): a randomised, double-blind trial. Lancet. 2009 Nov 28;374(9704):1840–8.
Related papers
La medicina tradizionale basa le sue scelte e soluzioni terapeutiche sulla dimostrazione della efficacia dei farmaci quale emerge dai risultati degli studi clinici controllati che selezionano le molecole più efficaci e dettano la strategia di impiego nei pazienti in cui si presume una maggiore efficacia. Nell’ambito di questa strategia di condotta è possibile identificare due [more info]
L’insostenibile leggerezza dell’essere, splendido romando di Milan Kundera, ha come tema principale la pesantezza esistenziale. Ogni persona vive una sola volta e non si ha mai la possibilità di valutare le proprie scelte, perciò diventa difficile capire se tutto ciò che si fa nella vita è giusto o sbagliato, perché non si ha modo di [more info]
Introduzione Le malattie cardiovascolari (CV) costituiscono una delle principali cause di mortalità in tutto il mondo. Secondo l’Organizzazione Mondiale della Sanità (OMS), nel 2019 circa il 32% delle morti globali è stato attribuito a malattie cardiovascolari (1). Tra queste, ruolo predominante gioca la malattia coronarica aterosclerotica, la quale rappresenta la prima causa di mortalità e [more info]